KOREA PHARMACEUTICAL TRADERS ASSOCIATION
개요
원료의약품을 수입하고자 하는 자는 소재지 관할지방식약청에 수입업 신고를 하여야 하며, 수입하려는 제품에 대해 식품의약품
안전처장의 품목허가(또는 신고)를 받아야 합니다. 이후 매 수입 시마다 한국의약품수출입협회장에게 전자무역문서로 표준통관
예정보고를 신청하여 요건확인을 받아 수입∙통관하여야 합니다. 다만, 의약품등의 제조업자가 자신이 제조하는 의약품등의 원료
로
사용하기 위하여 직접 원료의약품을 수입하는 경우에는 수입업 신고 및 수입품목 허가(신고) 대상에서 제외되나 원료의약품
을 수입하여 판매하는 경우에는 반드시 의약품등 수입업 신고를 하여야 합니다.
원료의약품이란?
합성, 발효, 추출 등 또는 이 방법들의 조합에 의하여 제조된 물질로서 완제의약품의 제조에 사용되는 것을 말합니다.
(의약품 제조 및 품질관리 기준)
관련규정
원료의약품 수입절차
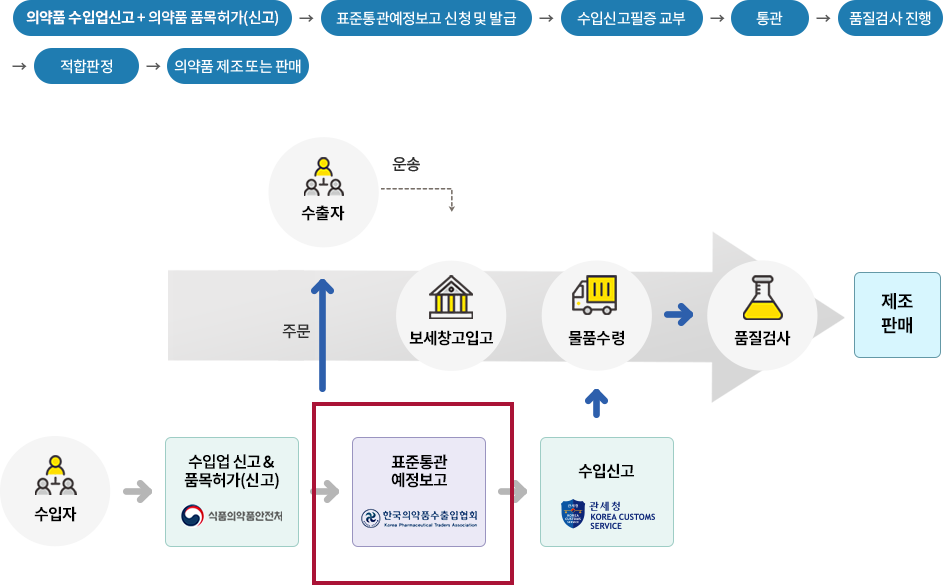
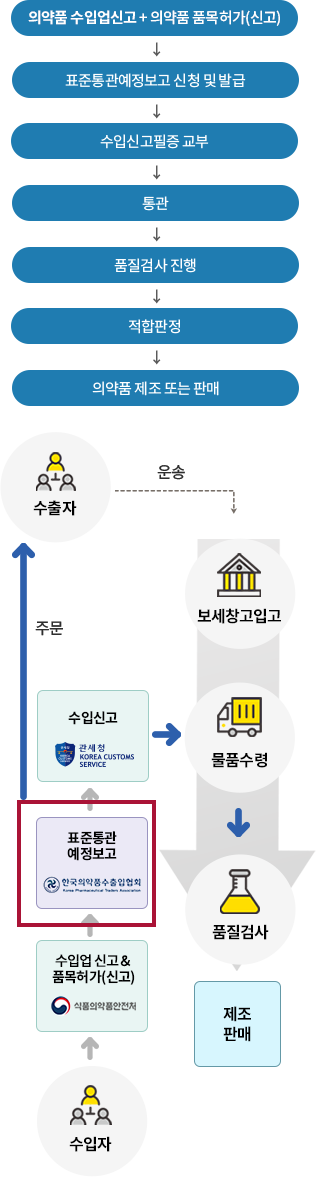
수입자 자격요건(‘가’ 또는 ‘나’에 해당하는 자)
가. 의약품 수입업 신고를 완료한 자
1
시설: 영업소 및 창고, 시험실(품질검사기관 위탁가능)2
인력: 수입관리자 및 안전관리책임자 각각 1인 이상3
품목허가(신고): 수입하려는 품목의 의약품 품목허가(신고) 1개 이상 *나. 의약품 제조업자
자사 의약품등의 원료로 사용하기 위하여 직접 원료의약품을 수입하는 경우만 해당합니다.
수입자 시설기준
영업소 및 창고의 조건
1
쥐∙해충 등을 막을 수 있는 시설2
저온 보관 및 빛가림을 위한 시설3
생물학적 제제의 보관시설4
마약 및 향정신성의약품의 보관시설5
보관방법이 정하여진 의약품등의 경우에는 그 보관조건을 유지할 수 있는 시설시험실(품질검사)
수입자는 시험실과 시험에 필요한 시설 및 기구를 갖추고 제조번호 별로 품질검사를 하여야 합니다. 다만 식약처장이 지정한 의약품 품질검사를 대행하는 검사 기관의 시설 및 기구를 이용하여 시험검사를 하는 경우에는 별도로 품질검사기관을 두지 아니할 수 있습니다. ※ 참고: 위탁품질검사기관 한국의약품시험연구원(TEL: 02-2162-8100)
의약품 허가·신고 방법
표준통관예정보고서 신청방법
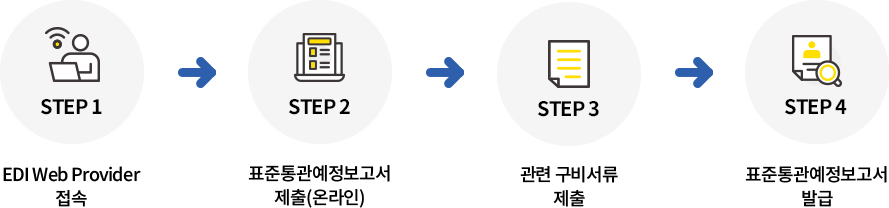

구비서류
* 의약품 제조용 원료물질(예: 원료의 원료, 중간체) 구비서류 안내
원료의 원료 및 중간체에 해당하는 물질의 경우 식약처에서 의약품에 해당된다는 유권해석을 받은 경우에만 신규로 수입이 가능합니다. 의약품 제조용 원료물질 유권해석 여부 확인 바랍니다.
「수입 원료의약품 GMP 증명서 요건 세부지침」및 질의응답
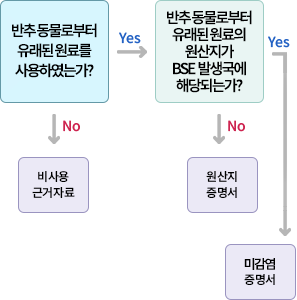
BSE(Bovine Spongiform Encephalopathy) 적용 기준은?
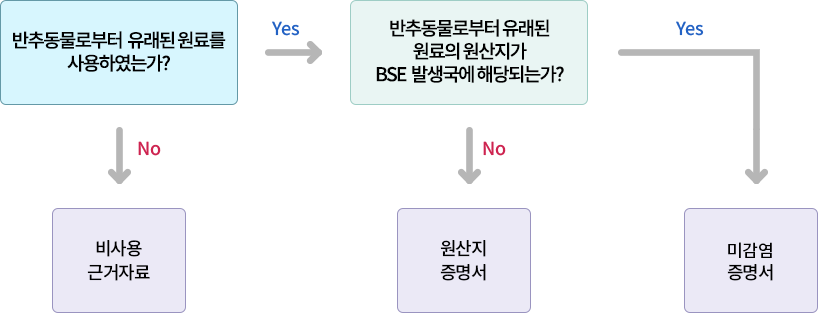
문의
| 구분 | 담당자 | 연락처 |
|---|---|---|
| 원료의약품 | 정다운 책임매니저 | 02-2162-8041 |
| 김보라 책임매니저 | 02-2162-8042 |